
Ethics Committee
申請方法の確認と様式
- HOME
- 生命科学・医学系研究倫理委員会
- 申請方法の確認と様式
申請方法の確認と申請様式のダウンロード
①新規審査申請
フローチャートで研究への参加形態および手続きの方法(A~H)を確認し、各申請で必要な資料をダウンロードのうえ作成してください。作成後、倫理審査申請システムより申請してください。(A~E,Hの場合)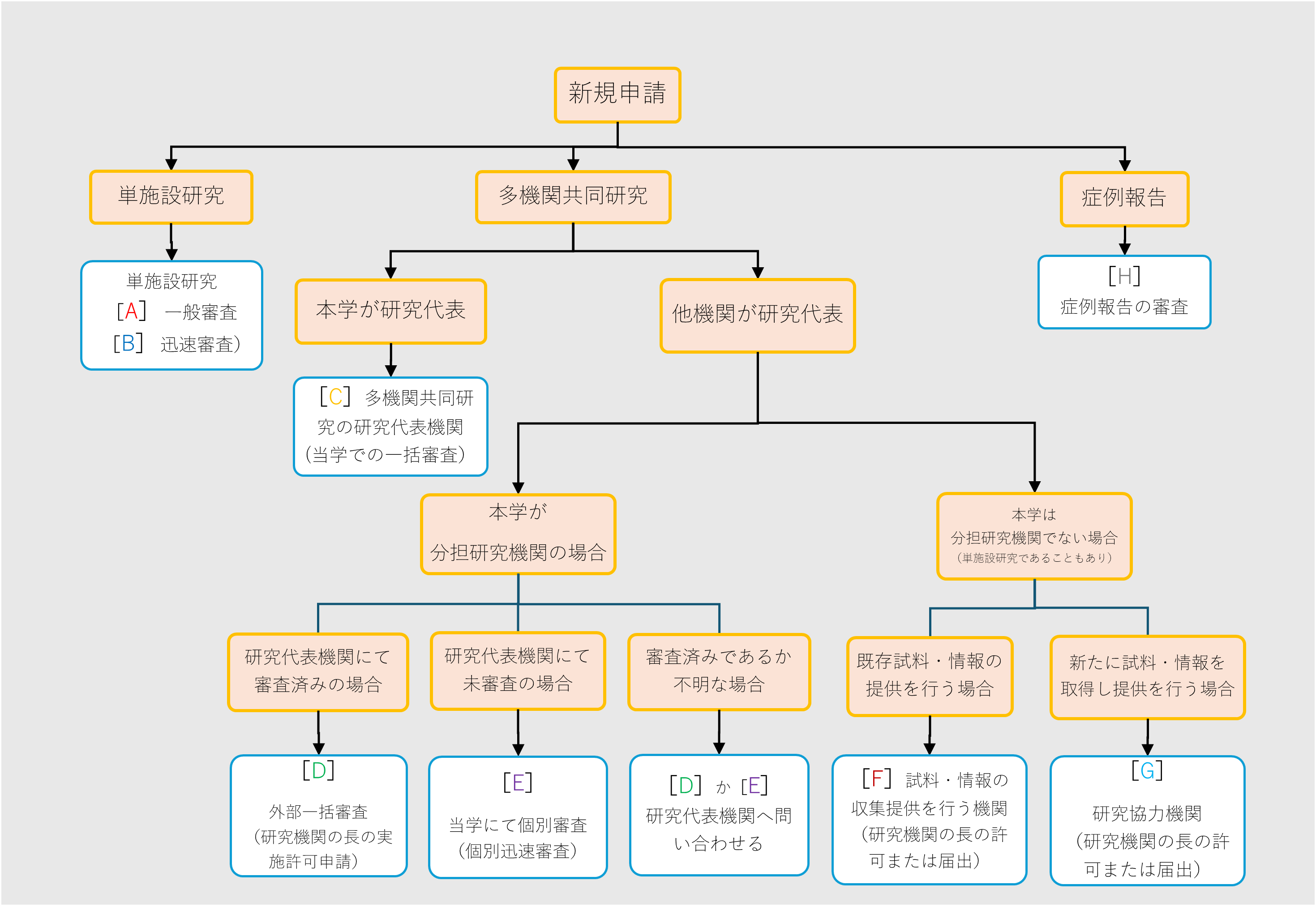
[A]単施設研究・一般審査(侵襲または介入または企業関与研究)
*は適宜選択して利用してください。
| No. | 書類名 | DL |
| 1 | 新規審査申請書 | システムへ入力 |
| 2 | 研究実施計画書(介入研究用)* | Word |
| 研究実施計画書(前向き観察研究用)* | Word | |
| 研究実施計画書(後ろ向き観察研究用)* | Word | |
| 3 | 同意説明文書、同意書・同意撤回書* | Word |
| 同意説明文書、同意書・同意撤回書(健常者用)* | Word | |
| 4 | 情報公開文書(オプトアウト文書)(単施設用)* | Word |
| 情報公開文書(オプトアウト文書)(提供を受ける用・自機関利用有り)* | Word | |
| 情報公開文書(オプトアウト文書)(提供を受ける用・自機関利用なし)* | Word | |
| 情報公開文書(オプトアウト文書)(提供を行う用)* | Word | |
| 5 | (アセント文書) | アセント用 (Word) |
| 6 | (遺伝子の説明文書) | Word |
| 7 | (契約書案の写し(受託研究・企業関与研究等の場合)) |
※その他、医薬品・医療機器の添付文書、アンケート用紙、参考文献、募集ポスターなど、必要に応じて提出して下さい。
[B]単施設研究・迅速審査(侵襲または介入または企業関与研究以外の観察研究)
*は適宜選択して利用してください。
| No. | 書類名 | DL |
| 1 | 新規審査申請書 | システムへ入力 |
| 2 | 研究実施計画書(前向き観察研究用)* | Word |
| 研究実施計画書(後ろ向き観察研究用)* | Word | |
| 3 | 同意説明文書、同意書・同意撤回書* | Word |
| 同意説明文書、同意書・同意撤回書(健常者用)* | Word | |
| 4 | 情報公開文書(オプトアウト文書)(単施設用)* | Word |
| 情報公開文書(オプトアウト文書)(提供を受ける用・自機関利用有り)* | Word | |
| 情報公開文書(オプトアウト文書)(提供を受ける用・自機関利用なし)* | Word | |
| 情報公開文書(オプトアウト文書)(提供を行う用)* | Word | |
| 5 | (アセント文書) | アセント用 (Word) |
| 6 | (遺伝子の説明文書) | Word |
| 7 | (契約書案の写し(受託研究・企業関与研究等の場合)) |
※その他、医薬品・医療機器の添付文書、アンケート用紙、参考文献、募集ポスターなど、必要に応じて提出して下さい。
[C]多機関共同研究(当学が研究代表機関の場合)・本学での中央一括審査
当学にて他の研究機関を一括審査する場合は[A]または[B]に加えて、下記一括審査3点セットの書類を提出してください。
| No. | 書類名 | DL |
| 8 | 倫理審査依頼申請書(共同研究機関の一括審査申請書) | Word |
| 9 | 研究機関チェックシート | Word |
| 10 | 研究者等リスト(研究責任者1名のみの場合は提出不要) | Word |
| 11 | (契約書案の写し(企業との共同研究の場合)) |
※「研究機関チェックシート」「研究者等リスト」は、共同研究機関に作成を依頼してください。
※「研究機関チェックシート」は、研究責任者による自署のうえ、PDFにて提出が必要です。
※「倫理審査依頼申請書」は、本学の研究責任者が作成してください。
[D]多機関共同研究(本学が分担研究機関で他の機関に審査を委託する場合)・研究機関の長の実施許可申請
研究代表機関において審査が承認となりましたら、以下の書類をご添付いただき申請してください。
| No. | 書類名 | DL |
| 1 | 新規実施許可申請書 | システムへ入力 |
| 2 | 代表研究機関にて審査済みの審査結果通知書 (本学が一括審査されたことがわかるもの) |
|
| 3 | 代表研究機関にて審査済みの研究計画書 (本学が共同研究機関であることが記載されているもの) |
|
| 4 | 代表研究機関にて審査済みのIC書類 (同意説明文書・オプトアウト文書など)※ |
|
| 5 | (その他代表研究機関にて審査済みの資料) |
※本学にてオプトアウトを行う場合は、本学用に個別入力部分を修正して提出してください。
[E]多機関共同研究(本学が分担研究機関で本学による個別審査を行う場合)
| No. | 書類名 | DL |
| 1 | 新規審査申請書 | システムへ入力 |
| 2 | 他の施設が主任となる多機関共同研究に個別審査により参加する場合の研究実施計画書 | Word |
| 3 | 代表研究機関にて審査済みの審査結果通知書 | |
| 4 | 代表研究機関にて審査済みの研究計画書 (本学の研究参加がわかるもの) |
|
| 5 | 代表研究機関にて審査済みのIC書類 (同意説明文書・オプトアウト文書など)※ |
|
| 6 | (その他代表研究機関にて審査済みの資料) |
※同意説明文書、オプトアウトは、本学用に個別入力部分を修正して提出してください。
[F][G]既存試料・情報の収集・提供を行う機関/研究協力機関・研究機関の長の許可申請または届け出
他の研究機関へ試料・情報の提供のみ(当学は研究機関に該当しない)の場合は下記の必要書類を作成の上、代表機関で作成された計画書および審査結果通知書と一緒に、医学部研究倫理事務局へメールで提出して下さい。医学部長許可を得た後(もしくは報告を行った後)、提供開始となります。
| No. | 書類名 | DL |
| 1 | 他の研究機関への試料・情報の提供に関する(申請・報告)書 | Word |
| 2 | 日本国外にある機関への試料・情報の提供に関する(申請・報告)書 | Word |
| 3 | 代表研究機関にて審査済みの審査結果通知書 | |
| 4 | 代表研究機関にて審査済みの研究計画書 (本学の研究参加がわかるもの) |
|
| 5 | 代表研究機関にて審査済みのIC書類 (同意説明文書・オプトアウト文書など)※ |
|
| 6 | (その他代表研究機関にて審査済みの資料) |
※同意説明文書、オプトアウトは、本学用に個別入力部分を修正して提出してください。
※新たに試料・情報の収集・提供を行う場合(研究協力機関)は、本学では同意をとることはできませんので、同意説明文書の提出は不要です。
※基本第1月曜日開催の委員会にて審査または報告を行います。
[H]症例報告の審査
症例報告※は、「人を対象とする生命科学・医学系研究に関する倫理指針」の対象外であり、倫理審査は基本的には不要です。ただし、症例報告を学会・論文発表するにあたり、倫理審査委員会の審査が必要とされる場合にご申請ください。
※症例報告:他の医療従事者への情報共有を図るため、所属する機関内の症例検討会、機関外の医療従事者同士の勉強会や関係学会、医療従事者向け専門誌等で個別の症例を報告すること(「人を対象とする生命科学・医学系研究に関する倫理指針ガイダンス/第2 用語の定義」5ページ)
倫理審査申請システムより申請してください。
| No. | 書類名 | DL |
| 1 | 症例報告倫理審査申請書 | システムへ入力 |
| 2 | 抄録、投稿原稿 | |
| 3 |
(症例報告 説明・同意文書) |
Word |
※月2回の迅速審査にて書類審査を行います。
②変更審査申請(原則 書類審査)
臨床研究の変更申請は原則として新規申請を行った 倫理審査委員会にて行う必要があります。倫理審査申請システムより変更申請をしてください。変更のある書類のみ、修正箇所を赤字にしてご提出ください。| No. | 書類名 | DL |
| 1 | 変更審査申請書 | システムへ入力 |
| 2 | (変更対照表) | Word |
| 3 | (倫理審査依頼申請書(共同研究機関の一括審査申請書)) | Word |
| 4 | (研究機関チェックシート) | Word |
| 5 | (研究分担者等リスト) | Word |
※変更箇所が多い場合は変更対照表に変更前、変更後を記載の上、提出してください。
※本学が多機関共同研究の研究代表機関で一括審査を行った研究の変更の場合
・共同研究機関の研究分担者に変更がある場合は、「研究分担者等リスト」を更新して一緒にご提出ください。
・「研究機関チェックシート」は、研究試料・情報の保管場所が変更になった等、記載内容に変更があった場合のみ再提出してください。研究責任者が変更になったのみの場合は、提出不要です。
・「倫理審査依頼申請書(共同研究機関の一括審査申請書)」は、共同研究機関が追加になった場合、追加になった研究機関について記載のうえ、ご提出ください。
※本学が多機関共同研究の分担研究機関の場合は、変更審査結果通知書および審査済み資料一式もご提出ください。
③定期報告・終了報告・有害事象報告・その他報告
倫理審査申請システムより報告をしてください。| No. | 書類名 | DL |
| 31 | 実施状況報告書 | システムへ入力 |
| 33 | 重篤な有害事象に関する報告書(第一報、第二報) | システムへ入力 |
| 34 | 予測しない重篤な有害事象報告 | システムへ入力 |
| 35 | 研究[終了・中止]報告書 | システムへ入力 |
※研究責任者は、重篤な有害事象の発生を知った場合には、速やかに「重篤な有害事象に関する報告書(第一報)」の報告をしてください。また、原則として7日以内に、「重篤な有害事象に関する報告書(第二報)」を報告してください。
(信州大学医学部・附属病院 人を対象とする生命科学・医学系研究における重篤な有害事象発生時に関する手順書)
※「不適合報告」「逸脱報告」等の不適切事案に関しては、速やかに事務局へお問い合わせください。
