研究紹介(吉沢 隆浩)
2013.04.18 教職員紹介(2026.01.22更新)
希少疾病のモデル動物開発や実験動物の飼育方法向上に関するテーマで、研究を展開しています。このページでは、以下の内容について紹介しています。
研究テーマ
以下の2つの研究テーマをメインにしています。
1. 希少疾病の疾患モデル動物開発と病態メカニズム解明
[概要]
医療が発展した現代においても、病気のメカニズムが分からなかったり、治療法が確立されていない疾患は数多く存在します。特に、希少疾患はこれまでに6,000以上が特定され、患者数は全世界で3億人以上に上ると推定されています。しかし、それらの疾患の95%では治療法が確立されていません。そうした病気の治療法を開発するためには、まずは前臨床試験やその前段階の基礎研究において、病気のメカニズムや治療薬候補物質の効果などを十分に検討する必要があります。そのための手段として、AI等を用いたin silicoのスクリーニングや、培養細胞などを用いたin vitroでの解析および、疾患モデル動物を用いたin vivoでの解析など、理論(計算)、細胞、個体レベルの解析を組み合わせた多面的なアプローチが必要になります。特に、私達の体は多種類の細胞によって構成され、さらに体内の複数の臓器や組織が影響し合い協調することで、生命活動の絶妙なバランスが成り立っています。このことから、病気のメカニズムを探り治療法開発の糸口を掴むためには、疾患モデル動物等を用いた「生きた体でのメカニズムや効果の検証」が欠かせません。
私の研究の目的は、希少疾病の疾患モデル動物を樹立し、病態メカニズムの解明を行うことと、将来的な治療薬開発の際の薬効薬理試験に役立つような評価法を確立することおよび、実験動物を用いた治療実験により治療薬開発に貢献することにあります。特に、希少疾病では、患者も研究者も少ないことがしばしばあり、その病気の研究や治療法開発が思うように進まないことがあります。また、研究に必要な疾患モデル動物が、現時点では樹立されていない場合もあります。そうした病気の疾患モデル動物を作成・解析することで、病態解明研究や前臨床試験の前進を助け、一日も早い治療法開発に繋がればと考え、研究に取り組んでいます。
[現在取組んでいるテーマ]
以下の疾患の、疾患モデル動物開発・病態メカニズム解明・治療法探索
- 筋拘縮型エーラスダンロス症候群(mcEDS)
- 顔面肩甲上腕型筋ジストロフィー(FSHD)
- SYT14遺伝子変異による脊椎小脳変性症(共同研究)
[実験技術]
以下のような実験技術を有し、これらの手法を組み合わせて研究に用いています。
- マウス受精卵に対するCRISPR/Cas9を用いたゲノム編集による、遺伝性疾患モデルマウスの作出
- 疾患モデルマウスの生理学的解析(生理条件下や外的刺激に対する生体反応の解析)
- 疾患モデルマウスの病理学的解析(病理組織標本を用いた臓器/組織の病変の解析)
- 疾患モデルマウスの分子生物学的解析(臓器/組織における遺伝子やタンパクの発現レベル等の解析)
- 疾患モデル動物を用いた治療実験(薬物投与等による治療効果の解析)
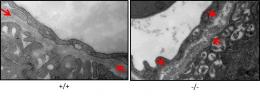
図:Chst14遺伝子欠損マウスの胎盤柔毛の毛細血管(透過型電子顕微鏡写真)
mcEDSの原因遺伝子であるChst14の欠損によって、毛細血管基底膜に断裂が認められた。(左:野生型、右:Chst14遺伝子欠損) (T.Yoshizawa et al. Glycobiology,28(2):80-89 2018.で発表)
2. 飼育環境や実験条件等が実験動物に与える影響
飼育環境を含む実験条件は、実験動物のコンディションに影響を与える重要な要因です。適切な飼育条件を維持することは、動物愛護の面から重要であることはもちろん、正確な実験データを得るためにも欠かせません。しかし、細かな飼育/実験条件は、研究室や実験者の経験に基づくさじ加減(客観的数値に基づかない経験則)によって調整される場合があり、再現性や効率の面で課題が残ります。そのため、本テーマでは、客観的根拠に基づいた適切な飼育管理を目指し、以下のような課題に取り組んでいます。
- 飼育ケージの床材の素材の違いがラットに与える影響
床敷き、金網、樹脂版の3種の異なる床材がラットの実験データに及ぼす影響について検討しました。
(吉沢隆浩、松本清司ら、日本実験動物学会第62回総会(2015年)で発表) - 輸送や手術およびケージ交換などの環境変化や身体的負荷がマウス/ラットの活動量に与える影響
新型活動量計nano tag®(キッセイコムテック/アコーズ)を用いた活動量の連続測定によって、手術や、ブリーダーからの輸送、ケージ交換などがラットの活動量に与える影響を解析し、活動量の面から順化回復期間の重要性を明らかにしました。
(T.Yoshizawa, K.Matsumoto et al. Experimental Animals, 68(3):277-283 2019.で発表) - 遺伝背景がChst14遺伝子欠損(KO)マウスの出生率に及ぼす影響
mcEDSのモデル動物として期待されつつも出生率の低さから解析が困難であったChst14 KOマウスの出生率に、遺伝背景が関係していることを見出し、BALB/c系統への戻し交配によって出生率の改善に成功しました。
(S.Shimada, T.Yoshizawa et al. Experimental Animals, 69(4): 407-413 2020.で発表) - エンリッチメントが離乳率に与える影響 など
小動物用エンリッチメントの利用によって、Chst14 KOマウスの出生率が向上することが明らかになりました。
(嶋田新、吉沢隆浩ら、信州実験動物研究会第40回研究発表会(2023年)で発表)
(高橋有希、吉沢隆浩ら、第68回日本実験動物学会総会(2021年)で発表)
研究業績(受賞)
2013年度(当部門着任)以降に受賞した学会賞等を以下に紹介します。
- 第4回日本エーラス・ダンロス症候群(EDS)研究会 JEFA賞 (2023年12月2日)
「筋拘縮型EDSのモデルマウスによる破骨細胞分化誘導解析:骨病変の全容解明を目指して」
高橋有希、吉沢隆浩、小野史子、岳鳳鳴、古庄知己
(筋拘縮型エーラス・ダンロス症候群[mcEDS]の疾患モデルマウスを用いた骨の解析から、mcEDS患者と同様の骨の変形や脆弱性を認めました。さらに、進行性の骨変形に破骨細胞分化の違いが関与することが示唆されました。)
詳細はコチラをご覧ください。 - 日本実験動物学会 奨励賞 (2023年5月25日)
「筋拘縮型エーラスダンロス症候群の疾患モデル動物の開発と解析」
吉沢隆浩
(信州大学[古庄ら]から報告された新規疾患である筋拘縮型エーラス・ダンロス症候群[mcEDS]の疾患モデルマウスを樹立すべく、胎生期の解析、出生率改善、コンディショナルノックアウトマウスの樹立、ならびびに成獣を用いたmcEDS患者と類似の表現型を示すモデルの確立と治療実験を行いました。また、日本実験動物学会の評議員や編集委員等として、これまで実験動物科学領域への貢献に努めてきました。これらの幅広い業績が評価されるとともに、今後のさらなる発展と貢献を期待されての受賞となりました。)
詳細はコチラをご覧ください。 - 信州実験動物研究会第40回研究発表会 奨励賞 (2023年3月10日)
「環境エンリッチメントを用いたChst14 KOマウスの出生率改善方法の検討」
嶋田新、吉沢隆浩、岩渕忍、江崎真司、山中仁木、古庄知己
(mcEDSの疾患モデル動物として期待されつつも、出生率が低く解析が難しかったChst14 KOマウスの出生率改善方法を、詳細に検討しました。適切な遺伝背景と環境エンリッチメントの利用が出生率を改善することを解明し、動物愛護[使用数削減]とmcEDS研究の進展に貢献しました。)
詳細はコチラをご覧ください。 - 第8回日本筋学会学術集会 Young Investigator Award 優秀賞 (2022年8月6日)
「顔面肩甲上腕型筋ジストロフィーの治療法探索」
吉沢隆浩、富山愛隆、中澤博美、畑志織、柴直子、高谷智英、宮崎大吾、中田勉、柴祐司、中村昭則、古庄知己
(未だ治療法の開発されていない疾患である顔面肩甲上腕型筋ジストロフィーの疾患モデル動物の検討、治療薬候補物質のスクリーニング、疾患モデル動物へのヒット化合物投与による治療効果の解析といった一連の研究および、それによる将来的な治療法開発への可能性が評価されました。)
詳細はコチラをご覧ください。
研究業績(発表論文)
2013年度(当部門着任)以降に発表した論文(国際誌・査読有)の一覧を以下に紹介します。学会発表やその他の研究業績等に関する詳細はSOARをご覧ください。
2025年
- Involvement of membrane palmitoylated protein 6 (MPP6) in synapses of mouse cerebrum
Histochemistry and Cell Biology, 2025(May 13), Yurika Saitoh*, Sayaka Motofuji, Akio Kamijo, Tatsuo Suzuki, Takahiro Yoshizawa, Takeharu Sakamoto, Kiyokazu Kametani, Nobuo Terada*
(共著者) - Carbohydrate sulfotransferase 14 gene deletion induces dermatan sulfate deficiency and affects collagen structure and bowel contraction
PLOS One, 2025(May 6), Fumiko Ono, Yuki Takahashi, Shin Shimada, Shuji Mizumoto, Shinji Miyata, Yuko Nitahara-Kasahara, Shuhei Yamada, Takashi Okada, Tomoki Kosho, Takahiro Yoshizawa*
(最終著者、責任著者) - Becker muscular dystrophy mice showed site-specific decay of type IIa fibers with capillary change in skeletal muscle
eLife, 2025(Mar. 17), Daigo Miyazaki*, Mitsuto Sato, Naoko Shiba, Takahiro Yoshizawa, Akinori Nakamura*
(共著者) - Model animals and attempts to develop therapeutic drugs for facioscapulohumeral muscular dystrophy
Translational and RegulatorySciences (TRS), 2025(Feb. 18), Takahiro Yoshizawa*, Mitsuru Sasaki-Honda, Hidetoshi Sakurai, Tomoki Kosho
(筆頭著者、責任著者)
2023年
- Recent progress on genetically modified animal models for membrane skeletal proteins the 4.1 and MPP families
Genes,14(10):1942 2023(Oct. 15), Nobuo Terada*, Yurika Saitoh, Masaki Saito, Tomoki Yamada, Akio Kamijo, Takahiro Yoshizawa, Takeharu Sakamoto
(共著者) - Mouse Models of Musculocontractural Ehlers-Danlos Syndrome
Genes,14(2):436 2023(Feb. 08), Takahiro Yoshizawa*, Tomoki Kosho
(筆頭著者、責任著者) - Collagen Network Formation in In Vitro Models of Musculocontractural Ehlers-Danlos Syndrome
Genes,14(2):308 2023(Jan. 24), Ayana Hashimoto, Takuya Hirose, Kohei Hashimoto, Shuji Mizumoto, Yuko Nitahara-Kasahara, Shota Saka, Takahiro Yoshizawa, Takashi Okada, Shuhei Yamada, Tomoki Kosho, Takafumi Watanabe, Shinji Miyata*, and Yoshihiro Nomura
(共著者)
2022年
- Protective roles of MITOL against myocardial senescence and ischemic injury partly via Drp1 regulation
iScience,25(7):104582 2022(Jun. 11), Takeshi Tokuyama,Hideki Uosaki,Ayumu Sugiura,Gen Nishitai, Keisuke Takeda,Shun Nagashima,Isshin Shiiba,Naoki Ito,Taku Amo,Satoshi Mohri,Akiyuki Nishimura,Motohiro Nishida,Ayumu Konno,Hirokazu Hirai,Satoshi Ishido,Takahiro Yoshizawa,Takayuki Shindo,Shingo Takada,Shintaro Kinugawa,Ryoko Inatome and Shigeru Yanagi*
(共著者) - Polygenic control of the wavy coat of the NCT mouse: involvement of an intracisternal A particle insertional mutation of the protease, serine 53 (Prss53) gene, and a modifier gene
Mammalian Genome,(33):451-464 2022(Jan. 24), Masayuki Mori*, Chang Liu, Takahiro Yoshizawa, Hiroki Miyahara, Jian Dai, Yuichi Igarashi, Xiaoran Cui, Ying Li, Xiaojing Kang, Keiichi Higuchi
(共著者)
2021年
- A new mouse model of Ehlers-Danlos syndrome generated using CRISPR/Cas9-mediated genomic editing
Disease Models & Mechanisms,14(12):dmm048963 2021(Dec. 23), Yuko Nitahara-Kasahara*, Shuji Mizumoto, Yukiko U Inoue, Shota Saka, Guillermo Posadas-Herrera, Aki Nakamura-Takahashi, Yuki Takahashi, Ayana Hashimoto, Kohei Konishi, Shinji Miyata, Chiaki Masuda, Emi Matsumoto, Yasunobu Maruoka, Takahiro Yoshizawa, Toshiki Tanase, Takayoshi Inoue, Shuhei Yamada, Yoshihiro Nomura, Shin'ichi Takeda, Atsushi Watanabe, Tomoki Kosho, Takashi Okada*
(共著者) - IQSEC2 deficiency results in abnormal social behaviors relevant to autism by affecting functions of neural circuits in the medial prefrontal cortex. Cells,10(10):2724 2021(Oct. 12), Anuradha Mehta, Yoshinori Shirai, Emi Kouyama-Suzuki, Mengyun Zhou, Takahiro Yoshizawa, Toru Yanagawa, Takuma Mori, Katsuhiko Tabuchi*
(共著者) - Risperidone mitigates enhanced excitatory neuronal function and repetitive behavior caused by an ASD-associated mutation of SIK1, Frontiers in Molecular Neuroscience,14(706494) 2021(May 27), Moataz Badawi, Takuma Mori*, Taiga Kurihara, Takahiro Yoshizawa, Katsuhiro Nohara, Emi Kouyama-Suzuki, Toru Yanagawa, Yoshinori Shirai, Katsuhiko Tabuchi*
(共著者)
2020年
- Systematic investigation of the skin in Chst14−/− mice: a model for skin fragility in musculocontractural Ehlers-Danlos syndrome caused by CHST14 variants (mcEDS-CHST14), Glycobiology, 31(2):137-150 2020(Jun. 27), Takuya Hirose, Shuji Mizumoto, Ayana Hashimoto, Yuki Takahashi, Takahiro Yoshizawa, Yuko Nitahara-Kasahara, Naoki Takahashi, Jun Nakayama, Kazushige Takehana, Takashi Okada, Yoshihiro Nomura, Shuhei Yamada, Tomoki Kosho*, Takafumi Watanabe*
(共著者) - Backcrossing to an Appropriate Genetic Background Improves the Birth Rate of Carbohydrate Sulfotransferase 14 Gene-deleted Mice, Experimental Animals, 69(4): 407-413 2020(June 10), Shin Shimada, Takahiro Yoshizawa*, Yuki Takahashi, Yuko Nitahara-Kasahara, Takashi Okada, Yoshihiro Nomura, Hitoki Yamanaka, Tomoki Kosho, Kiyoshi Matsumoto
(責任著者。遺伝背景がChst14遺伝子欠損マウスの出生率に影響を与えることを明らかにしました。これにより、これまで困難であったChst14遺伝子欠損マウスの成獣を用いた解析が可能になり、新型エーラスダンロス症候群[mcEDS]の病態解明研究の加速が期待されます。)
2019年
- Recent Advances in the Pathophysiology of Musculocontractural Ehlers-Danlos Syndrome, Genes,11(1), 43 2019(Dec. 29), Tomoki Kosho*, Shuji Mizumoto, Takafumi Watanabe, Takahiro Yoshizawa, Noriko Miyake, and Shuhei Yamada
(共著者) - Cutting Edge: TAK1 Safeguards Macrophages against Proinflammatory Cell Death. The Journal of Immunology,203 (4):783-788 2019(Jun. 26), Hideki Sanjo*, Jun Nakayama, Takahiro Yoshizawa, Hans Joerg Fehling, Shizuo Akira and Shinsuke Taki
(共著者) - Continuous Measurement of Locomotor Activity During Convalescence and Acclimation in Group-Housed Rats, Experimental Animals,68(3):277-283 2019(Feb. 13), Takahiro Yoshizawa*, Shin Shimada, Yoshito Takizawa, Tsuyoshi Makino, Yasuhide Kanada, Yoshiharu Ito, Toshiaki Ochiai, and Kiyoshi Matsumoto
(筆頭著者、責任著者。新型活動量計nano tag®の実証試験を行い、装置の有用性を明らかにしました。また、輸送や手術などの負荷後のラットに対する、順化/回復期間の重要性を活動量の面から明らかにしました。)
2018年
- Evaluation of Necessity of 1-year Toxicity Study in Dogs - development of the New Tiered Approach for Toxicity Studies of Pesticide Considering Species Difference in "toxicity profile" and "toxicity dose-response", Food Safety 2018(May 31), Atsushi Ono*, Takahiro Yoshizawa, Kiyoshi Matsumoto
(共著者) - Vascular abnormalities in the placenta of Chst14-/- fetuses: implications in the pathophysiology of perinatal lethality of the murine model and vascular lesions in human CHST14/D4ST1 deficiency, Glycobiology,28(2):80-89 2018(Jan. 05), Takahiro Yoshizawa, Shuji Mizumoto, Yuki Takahashi, Shin Shimada, Kazuyuki Sugahara, Jun Nakayama, Shin'ichi Takeda, Yoshihiro Nomura, Yuko Nitahara-Kasahara, Takashi Okada, Kiyoshi Matsumoto, Shuhei Yamada, and Tomoki Kosho
(筆頭演者、責任著者。新型エーラスダンロス症候群[mcEDS]のモデル動物として期待されるChst14遺伝子欠損マウスの解析を行い、胎盤柔毛の毛細血管に異常が認められることを明らかにしました。これにより、mcEDSの新たな病態メカニズムと、Chst14遺伝子欠損マウスの疾患モデル動物としての有用性が示唆されました。)
2016年
- Effects of Adrenomedullin on Doxorubicin-induced Cardiac Damage in Mice, Biological and Pharmaceutical Bulletin,39(5) 2016(Feb. 22), Takahiro Yoshizawa*, Sho Takizawa, Shin Shimada, Takeshi Tokudome, Takayuki Shindo, and Kiyoshi Matsumoto
(筆頭著者、責任著者)
2015年
- Differential roles of MMP-9 in early and late stages of dystrophic muscles in a mouse model of Duchenne muscular dystrophy, BIOCHIMICA ET BIOPHYSICA ACTA-MOLECULAR BASIS OF DISEASE,1852(10):2170-2182 2015(Oct.), Shiba Naoko, Miyazaki Daigo, Yoshizawa Takahiro, Fukushima Kazuhiro, Shiba Yuji, Inaba Yuji, Imamura Michihiro, Takeda Shin'ichi, Koike Kenichi, Nakamura Akinori*
(共著者)
2014年
- Adrenomedullin-RAMP2 System Suppresses ER Stress-Induced Tubule Cell Death and Is Involved in Kidney Protection, PLOS ONE,9(2):e87667 2014(Feb. 05), Uetake Ryuichi, Sakurai Takayuki, Kamiyoshi Akiko, Ichikawa-Shindo Yuka, Kawate Hisaka, Iesato Yasuhiro, Yoshizawa Takahiro, Koyama Teruhide, Yang Lei, Toriyama Yuichi, Yamauchi Akihiro, Igarashi Kyoko, Tanaka Megumu, Kuwabara Takashige, Mori Kiyoshi, Yanagita Motoko, Mukoyama Masashi, Shindo Takayuki*
(共著者)
連絡先
ラボ見学等のご希望がありましたら、以下の連絡先までお問合せください。
住所
〒390-8621 長野県松本市旭3-1-1
信州大学基盤研究支援センター動物実験支援部門
メールアドレス
tyoshizawa☆shinshu-u.ac.jp
※ メール送信の際には☆を@に変えてください。

 ページの先頭へ戻る
ページの先頭へ戻る