研究テーマ3
骨格筋の収縮におけるL型カルシウムチャネルとジャンクトフィリンの役割
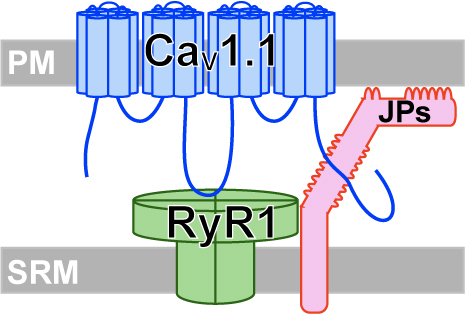
L型カルシウムチャネル(LTCC)は,骨格筋の収縮に必要不可欠な存在です。LTCCは細胞膜の電位変化を関知し,立体構造を変化させることで,物理的に結合している筋小胞体膜上のリアノジン受容体を開口させます。これにより,筋小胞体から大量のカルシウムイオンが放出され,筋細胞が収縮します。このプロセスを効率的に起こすために,骨格筋のLTCCは表面細胞膜と筋小胞体膜が近接する結合膜構造と呼ばれる部位に特異的に局在しています。LTCCの結合膜への局在は筋の正常な興奮収縮連関に必須ですが,その集積メカニズムの詳細はわかっていません。私たちはジャンクトフィリン(JP)と呼ばれる分子に注目し,このLTCCの結合膜構造への集積機構について解析を行いました。JPは表面細胞膜と筋小胞体膜を物理的に橋渡しし,結合膜構造を維持するタンパク質として知られています。
はじめに,培養細胞由来の筋管のJPの発現をRNA干渉により抑制すると,LTCCの結合膜への局在化が阻害され,カルシウム放出の減少などの機能異常が認められました。さらに詳細な解析を行った結果,LTCCの主要サブユニットタンパク質であるCaV1.1が,JPと物理的に結合していることが分かりました。
次に,JPのC末端欠失変異体(JP1ΔCT)を作製しました。この変異体は筋小胞体膜貫通部位を持たないため,結合膜に集積せず,細胞膜全体に分布するようになります。これを筋管に強制発現すると,LTCCの結合膜への集積が抑制されました。この結果は,JP1ΔCTがLTCCの正常な細胞内局在を阻害する,ドミンナントネガティブ様の作用を持つことを示しています。そこで,アデノ随伴ウイルスベクターを用いて,JP1ΔCTをマウス筋にin vivoで発現させる実験を行いました。その結果,JP1ΔCTを発現させた筋肉では,LTCCと内在性のJPの結合が阻害され,リアノジン受容体との結合も減少していました。これは骨格筋のLTCCの結合膜への集積に,JPとの結合が重要であることを示しています。また,生理学的な解析では,電気刺激に対するカルシウム応答や,筋の収縮力などが有意に減少していました。以上の結果から,LTCCのCaV1.1とJPとの物理的結合が,正常な筋収縮にとって必要であることが示唆されました。(Nakada et al., Proc Natl Acad Sci U S A. 2018 115: 4507-4512)