研究テーマ1
新たなAT1アンジオテンシン受容体修飾法による小児心不全治療法の開発
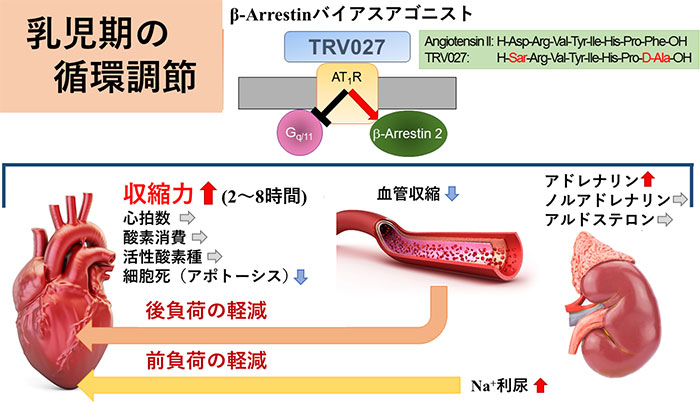
アンジオテンシンII(AngII)は、生体の循環調節に重要なホルモンです。AngIIが1型AngII受容体(AT1R)に結合すると、細胞内でGタンパク経路とβアレスチン経路の2つの経路が活性化します。AT1R/Gタンパク経路の活性化は、成人では高血圧・心肥大を生じやがて心不全の発症を誘発します。そのため、AT1Rのアンタゴニスト(AT1Rブロッカー:ARB)であるカンデサルタンなどは成人慢性心不全患者の生命予後を有意に改善することが知られています。一方、当教室はAT1R/βアレスチン経路が、新生児期・乳児期に限り、心筋細胞のL型Ca2+チャネルを活性化することを2017年に報告しました[Kashihara et al., J. Physiol. 2017]。L型Ca2+チャネルは、心臓の興奮収縮連関に重要なイオンチャネルであることから、上記知見はAT1R/βアレスチン経路が、幼若動物で強心作用を発揮することを示唆します。
そこで私たちは、AT1R/βアレスチン経路を特異的に活性化しつつ、AT1R/Gタンパク経路を抑制するβアレスチンバイアスAT1Rアゴニスト(BBA)の、in vivo及びin vitroでの作用について検討を行いました。生後5日以内の新生児マウスにペプチドBBAである「TRV027」を皮下投与すると、予想通り有意に心臓の収縮が高まりました。この作用は、投与後2時間でピークに達し、驚くことに8時間まで有意な強心作用を示しました[図1]。その一方で、TRV027は、多くの強心薬に認められるような不整脈、頻脈、心筋酸素消費増大、活性酸素種増加などの副作用を示しませんでした。さらにTRV027は、新生児マウス単離心室筋細胞のみならずヒトiPS細胞由来の心筋細胞(胎生~新生児期の心筋細胞の表現型を示す)でも、活動電位に伴う細胞内Ca2+濃度上昇を約2倍に強めました。最後にTRV027は、生後4~6日のヒト拡張型心筋症モデルマウス(cardiac troponin T(cTnT) K210欠損マウス;国際医療福祉大学 森本幸生博士作製)の病的心臓の収縮力も有意に上昇させました[図2]。以上のことから、AT1R/βアレスチン経路は、現在専用の治療薬のない小児心不全に対する新たな治療標的となる可能性が示されました。(*Kashihara, T., *Kawagishi, H. et al., β-Arrestin-Biased AT1 Agonist, TRV027 Causes a Neonatal-Specific Sustained Positive Inotropic Effect without Increasing Heart Rate. JACC: Basic to Translational Science, 5(11), 1057-1069, 2020 (*equal contribution))[図3]
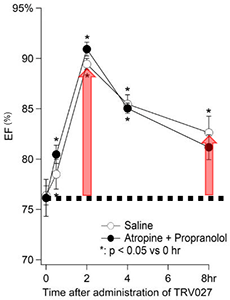
TRV027(3 mg/kg)投与による強心作用の誘導。投与後2時間でピークに達し、8時間後まで有意に収縮力が増大している。EF:左室駆出率(Ejection Fraction(%))
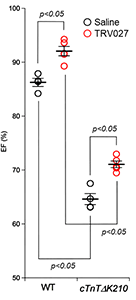
TRV027(3 mg/kg)投与2時間後における、生後4~6日の野生型(WT)、拡張型心筋症モデル(cTnTΔK210)マウスの左室駆出率。cTnTΔK210マウスの低下した心機能が、TRV027の投与により有意に改善した。