信州大学医学部 分子病態学教室
LOX-1と細胞との相互作用から細胞接着・炎症へHEADLINE
LOX-1と細胞接着
LOX-1の活性化は、血管内皮細胞で細胞接着分子の発現亢進を引き起こし、これにより白血球の血管内皮細胞への接着を促進していると考えられるが、LOX-1そのものが種々の細胞と直接相互作用することも明らかになっている。
老化赤血球・アポトーシス細胞
酸化LDLは、ある意味で生体内の老廃物であると考えられるので、LOX-1のような酸化LDL受容体が、やはり生体の老廃物ともいえる死細胞・老化細胞の認識に関わるのではないかという可能性を考えたことから、この研究は始まっている。当時、死細胞貪食の研究は脂質とは全く独立した領域の科学であったが、アポトーシスの初期段階でフォスファチジルセリンが(PS)が細胞膜表面に露出することが見出され(Martin, S.J. et al. J Exp Med 1995)、脂質研究との接点が生まれた。
通常、細胞膜リン脂質二重層は、外側の層と内側の層は対称ではなく、外側の層ではリン脂質は中性リン脂質のフォスファチジルコリン(PC)がほとんどで、酸性リン脂質のPSやフォスファチジルエタノールアミン(PE)は内側に偏在している。このリン脂質の細胞膜二重層での非対称性はATP依存性フリッパーゼの働きによって維持されている。しかし、アポトーシスの初期段階では、この非対称性が崩壊してPSが細胞外に露出する。非対称性の崩壊にはCa2+依存性のスクランブラーゼという酵素が関与すると考えられている。
では、LOX-1は死細胞、老化細胞を認識・貪食するのであろうか?LOX-1を介した細胞接着や細胞貪食作用を調べるため、内皮細胞やLOX-1発現細胞に、老化モデル赤血球、またはシクロヘキシミドでアポトーシスを誘導したHL-60細胞を添加すると、内皮細胞およびLOX-1発現細胞は、老化赤血球やアポトーシス細胞と結合して貪食した。一方、LOX-1を発現しない細胞では、このような細胞接着・細胞貪食は観察されなかった。このような接着・貪食はアポトーシス誘導の種類や細胞によらず、抗Fas抗体でアポトーシスさせたJarkat細胞、TNF-αでアポトーシスさせた内皮細胞も同様に接着した(Oka,
K. et al. Proc Natl Acad Sci USA 1998)。
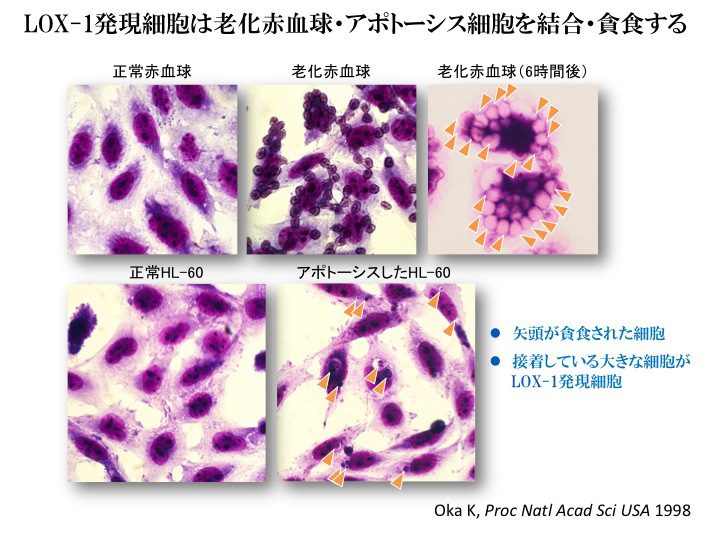
そして、LOX-1発現細胞は未処置の赤血球やHL-60細胞とは結合しなかったことから、LOX-1は老化やアポトーシスに伴って起こる細胞表面の変化を認識していると考えられた。そこで、リン脂質とLOX-1の関係を解析した。LOX-1発現細胞と老化赤血球・アポトーシス細胞の結合は、PSリポソームによって阻害されるが、PCリポソームやPEリポソームの影響を受けないことから、LOX-1は細胞外に露出したPSを認識していることが示唆された。また、ここで用いた老化モデル赤血球では、老化処置にしたがってPSの細胞表面への露出と、LOX-1の結合性の増加が並行して起きていた。
さらに、LOX-1とリン脂質の直接の結合実験から、LOX-1はPCやPEとは結合しないが、PSとCa2+依存的に直接結合することが明らかになった(Murphy,
J.E. et al. Biochem J 2006)。これらのことから、LOX-1は細胞膜リン脂質の中でもPSと特異的に結合することで、老化細胞やアポトーシス細胞の選択的な貪食に関与していると考えられる。
活性化血小板
PSの細胞外への露出は、細胞の老化やアポトーシスだけではなく、血小板の活性化でも生じる。このPSは、血液凝固因子の補因子として血液の凝固を促進する。私達は、LOX-1がPS露出細胞と結合することから、内皮細胞と活性化血小板が接着し、血栓形成などに関係しているのではないかと考えて検討を行った。
ADPで刺激した血小板を、培養内皮細胞に添加すると、血小板は内皮細胞と接着した後、貪食される像が観察された。同様の細胞接着・貪食はLOX-1発現細胞でも観察されたが、LOX-1を発現しない細胞は血小板と結合しなかった(Kakutani, M. et al. Proc Natl Acad Sci USA 2000)。
血小板とLOX-1発現細胞の結合は、酸化LDLやLOX-1抗体の添加によって阻害されたが、未変性LDLの影響を受けなかった。血小板の接着はまた、PS結合タンパク質アネキシンVやPSリポソームの添加によっても抑制されたが、PCリポソームの影響は受けなかった。以上の結果から、血小板の接着においてLOX-1とPSが結合していることが明らかになった。また、トロンビンやコラーゲンで血小板を活性化させると、その添加量に応じてLOX-1発現細胞への結合が亢進することから、血小板活性化に伴うPSの露出をLOX-1は認識していると考えられた。
また、活性化血小板を内皮細胞に接着させると、内皮からのエンドセリン-1(ET-1)の分泌がLOX-1依存的に亢進した。これはそのほかの実験結果から、血小板より放出された活性物質によるものではなく、細胞の接着自体によって引き起こされると考えられた。すなわち、LOX-1を介した細胞接着そのものが細胞への刺激になっていると考えられた。
LOX-1と白血球の相互作用から炎症へ
次にLOX-1の炎症における役割を、エンドトキシンであるリポポリサッカライド(LPS)をラットに投与するモデルで検討した。LPSを低濃度(0.5 mg/kg)で投与するブドウ膜炎モデルでは、網膜細静脈の内皮細胞におけるLOX-1の発現は、LPS投与12時間後で著明に亢進していた。眼房水中への白血球の浸潤とタンパク質の漏出はLPS投与24時間後に最大となったが、LPSと同時に抗LOX-1抗体を処置することで、これらは抑制された。
また、白血球の流量が最大になるLPS投与20時間後に、網膜血管における白血球のローリングと接着を測定した。白血球は内皮と相互作用することでローリングを始め、最終的には内皮に接着するが、LPSと同時に抗LOX-1抗体を投与すると、白血球のローリングの速度が速くなり、ローリングしている細胞数も減少した(Honjo,
M. et al. Proc Natl Acad Sci USA 2003)。
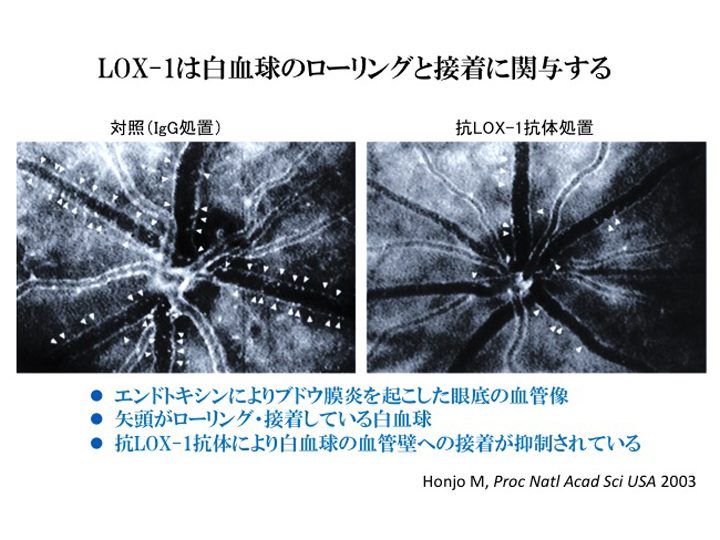
LOX-1が白血球を接着するかどうか調べるため、ヒト好中球を用い、in vitroの流れ条件下で接着実験を行った。好中球はLOX-1を固相化したスライドには接着したが、IgGを固相化したスライドには結合しなかった。抗LOX-1抗体の添加によって好中球の接着数が減少することから、LOX-1が好中球と直接結合することが明らかになった。これらの結果は、ブドウ膜炎モデルで観察されたLOX-1依存的な白血球のローリング・接着・浸潤を反映していると考えられる。
一方、敗血症を高濃度LPS(2 mg/kg)投与により誘導したラットは、1時間以内に白血球数の減少を起こし、24時間以内に70%が死に至った。しかし、抗LOX-1抗体をLPSと同時投与すると、白血球の減少は抑制され、全ての個体が生存した。現在、敗血症やSIRS(Systemic Inflammatory response syndrome)の治療にはプロテインCの投与があるが、その効果は必ずしも充分とはいえない。LOX-1の阻害は、敗血症やSIRSに対しての新しい効果的な治療法となる可能性がある。
関節炎
関節リウマチ(RA)は炎症性細胞の浸潤を伴う慢性関節炎である。関節リウマチと動脈硬化の関係は古くから知られており、疫学的にも、関節リウマチ患者で冠動脈疾患の発症率が上昇することが報告されている。また、関節リウマチ患者の滑膜や関節液中に酸化LDLが検出されることから、関節炎におけるLOX-1の役割について検討を行った。
まず、起炎物質であるザイモザンをラット膝関節に注射して関節炎を誘発した。LOX-1の発現は誘導6時間後から静脈および平滑筋で観察され、24時間後にはほぼ全ての静脈および細静脈で発現が認められた。LOX-1の発現は滑膜および軟骨でも観察されたが、動脈では認められなかった。また、軟骨における酸化LDLの蓄積は誘導6時間後から認められ、72時間後に至るまで増加を示した。
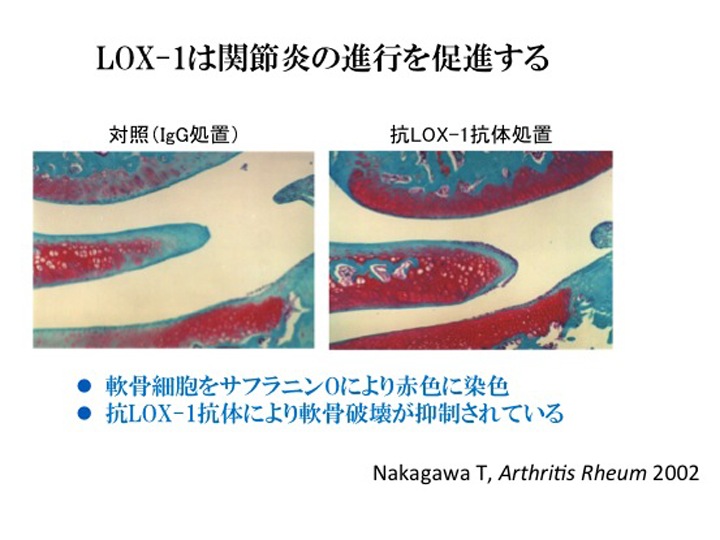
関節肥大は誘導3時間後から認められ、24時間後には関節径が最大となったが、抗LOX-1抗体処置により、誘導24時間後の関節肥大は最大34%抑制され、関節腔への白血球の浸潤も減少していた。また、誘導7日後の軟骨破壊、滑膜の肥厚も抑制されており、LOX-1の阻害が急性期および亜急性期の炎症を抑制することが明らかになった(Nakagawa,
T. et al. Arthritis Rheum 2002)。
その後、酸化LDLと関節軟骨のLOX-1の結合がNF-κBの活性化や活性酸素種の産生、マトリクスメタロプロテアーゼ3(MMP-3)の発現を誘導すること、関節軟骨に伸展ストレスを負荷するとLOX-1の発現が増加し、酸化LDL依存的な細胞死が促進されることがわかった(Nishimura, S. et al. Osteoarthritis Cartilage 2004; Kakinuma, T. et al. Arthritis Rheum 2004; Akagi, M. et al. J Orthop Res 2006)。
さらにヒトにおいて、変形性関節症(OA)患者の軟骨でLOX-1の発現および酸化LDLの蓄積が増加しており、両者は共局在していることが明らかになった。LOX-1や酸化LDLが陽性の細胞数は、関節炎の進展度を表すMankinスコアと正の相関を示した(Akagi, M. et al. Osteoarthritis Cartilage 2007)。このようなことから、ヒトの関節炎でもLOX-1と酸化LDLが病態の進行に関わっており、LOX-1が治療標的になり得る可能性が考えられる。
参考文献
Oka, K., Sawamura, T., Kikuta, K., Itokawa, S., Kume, N., Kita, T. and Masaki, T.: Lectin-like oxidized low-density lipoprotein receptor 1 mediates phagocytosis of aged/apoptotic cells in endothelial cells. Proc Natl Acad Sci USA, 95:9535-9540, 1998.
Martin, J.S. et al.: Early redistribution of plasma membrane phosphatidylserine is a general feature of apoptosis regardless of the initiating stimulus: inhibition by overexpression of Bcl-2 and Ab1. J Exp Med, 182:1545-1556, 1995.
Murphy, J.E., Tacon, D., Tedbury, P.R., Hadden, J.M., Knowling, S., Sawamura, T., Peckham, M., Phillips, S.E.V., Walker, J.H. and Ponnambalam, S.: LOX-1 scavenger receptor mediates calcium-dependent recognition of phosphatidylserine and apoptotic cells. Biochem J, 393;107-115, 2006.
Kakutani, M., Masaki, T. and Sawamura, T.: A platelet-endothelium interaction mediated by lectin-like oxidized low-density lipoprotein receptor-1. Proc Natl Acad Sci USA, 97:360-364, 2000.
Honjo, M., Nakamura, K., Yamashiro, K., Kiryu, J., Tanihara, H., McEvoy, L. M., Honda, Y., Butcher, E. C., Masaki, T. and Sawamura, T.: Lectin-like oxidized LDL receptor-1 is a cell-adhesion molecule involved in endotoxin-induced inflammation. Proc Natl Acad Scie USA, 100:1274-1279, 2003.
Nakagawa, T., Akagi, M., Hoshikawa, H., Chen, M., Yasuda, T., Mukai, S., Ohsawa, K., Masaki, T., Nakamura, T. and Sawamura, T.: Lectin-like oxidized low-density lipoprotein receptor 1 mediates leukocyte infiltration and articular cartilage destruction in rat zymosan-induced arthritis. Arthritis Rheum, 46:2486-2494, 2002.
Nishimura, S., Akagi, M., Yoshida, K., Hayakawa, S., Sawamura, T., Munakata, H. and Hamanishi, C.: Oxidized low-density lipoprotein (ox-LDL) binding to lectin-like ox-LDL receptor-1 (LOX-1) in cultured bovine articular chondrocytes increases production of intracellular reactive oxygen species (ROS) resulting in activation of NF-kappaB. Osteoarthritis Cartilage, 12:568-576, 2004.
Kakinuma, T., Yasuda, T., Nakagawa, T., Hiramitsu, T., Akiyoshi, M., Akagi, M., Sawamura, T. and Nakamura, T.: Lectin-like oxidized low-density lipoprotein receptor 1 mediates matrix metalloproteinase 3 synthesis enhanced by oxidized low-density lipoprotein in rheumatoid arthritis cartilage. Arthritis Rheum, 50:3495-3503, 2004.
Akagi, M., Nishimura, S., Yoshida, K., Kakinuma, T., Sawamura, T., Munakata, H. and Hamanishi, C.: Cyclic tensile strech load and oxidized low density lipoprotein synergistically induce lectin-like oxidized LDL receptor-1 in cultured bovine chondrocytes, resulting in decreased cell viability and proteoglycan synthesis. J Orthop Res, 24:1782-1790, 2006.
Akagi, M., Kanata, S., Mori, S., Itabe, H., Sawamura, T. and Hamanishi, C.: Possible involvement of the oxidized low-density lipoprotein/lectin-like oxidized low-density lipoprotein receptor-1 system in pathogenesis and progression of human osteoarthritis. Osteoarthritis Cartilage, 15:281-290, 2006.
研究概要
酸化LDL受容体LOX-1の発見
LOX-1とCRP
LOX-1に結合する内因性のリポ蛋白質
LOX-1ブロッカーの開発
LOX-1を用いた診断技術の開発